Химические уравнения 8. Решение типовых задач по химии. Расчет состава смеси по уравнению химической реакции
Закон сохранения массы веществ, открытый М. В. Ломоносовым в 1748 г., гласит:
Материальными носителями массы веществ являются атомы химических элементов, из которых состоят как вступившие в реакцию вещества (реагенты), так и образовавшиеся в результате её новые вещества (продукты реакции). Поскольку при химических реакциях атомы не образуются и не разрушаются, а происходит лишь их перегруппировка, то становится очевидным справедливость открытого М. В. Ломоносовым и подтверждённого позднее А. Лавуазье закона.
В справедливости закона сохранения массы веществ можно легко убедиться на простом опыте. Поместим в колбу немного красного фосфора, закроем её пробкой и взвесим на весах (рис. 96). Затем колбу осторожно нагреем. О том, что произошла химическая реакция, можно определить по появлению в колбе густого белого дыма, состоящего из оксида фосфора (V), который образовался при взаимодействии фосфора с кислородом. При повторном взвешивании колбы с продуктами этой реакции мы убедимся, что масса веществ в колбе не изменилась, хотя и произошло превращение фосфора в его оксид.
Рис. 96.
Экспериментальная проверка закона сохранения массы веществ:
а - взвешивание колбы с фосфором до реакции; б - горение фосфора в закрытой колбе; в - взвешивание колбы с продуктом реакции
Этот же вывод будет нами сделан и при проведении ещё одного простого, но очень наглядного опыта. В специальный сосуд нальём отдельно соляную кислоту и раствор щёлочи, например гидроксида натрия (рис. 97). К раствору щёлочи добавим несколько капель индикатора - фенолфталеина, отчего раствор окрасится в малиновый цвет. Закроем прибор пробкой, уравновесим гирями на весах, отметим массу, а затем сольём растворы. Малиновая окраска исчезнет, потому что кислота и щёлочь прореагировали друг с другом. Масса же сосуда с полученными продуктами реакции не изменилась.

Рис. 97.
Опыт, подтверждающий закон сохранения массы вещества
Аналогичное наблюдение сделал и автор закона сохранения массы веществ М. В. Ломоносов, который проводил опыты в запаянных стеклянных сосудах, «дабы исследовать, прибывает ли вес металла от чистого жару», и обнаружил, что «без пропущения внешнего воздуха вес металлов остаётся в одной мере».
На основании этого закона пишут химические предложения, т. е. составляют уравнения химических реакций с помощью химических слов - формул.
В левой части уравнения записывают формулы (формулу) веществ, вступивших в реакцию, соединяя их знаком «плюс». В правой части уравнения записывают формулы (формулу) образующихся веществ, также соединённых знаком «плюс». Между частями уравнения ставят стрелку. Затем находят коэффициенты - числа, стоящие перед формулами веществ, чтобы число атомов одинаковых элементов в левой и правой частях уравнения было равным.
Запишем, например, уравнение реакции водорода с кислородом. Сначала составим схему реакции - укажем формулы веществ, вступающих в реакцию (водород Н 2 и кислород O 2) и образующихся в результате её (вода Н 2 O), и соединим их стрелкой:
Н 2 + O 2 → Н 2 O (рис. 98, а).

Рис. 98.
Составление уравнения реакции взаимодействия водорода и кислорода
Так как число атомов кислорода в левой части вдвое больше, чем в правой, запишем перед формулой воды коэффициент 2:
Н 2 + O 2 → 2Н 2 O (рис. 98, б).
Но теперь в правой части уравнения стало четыре атома водорода, а в левой их осталось два. Чтобы уравнять число атомов водорода, запишем перед его формулой в левой части коэффициент 2. Так как мы уравняли число атомов каждого элемента в левой и правой частях уравнения, заменим стрелку на знак равенства:
2Н 2 + O 2 = 2Н 2 O (рис. 98, в).
Теперь, наверное, вам понятно, почему такую запись называют уравнением (рис. 99).

Рис. 99.
Закон сохранения массы веществ на примере реакции, уравнение которой 2Н 2 + O 2 = 2Н 2 O
Для составления уравнений химических реакций, кроме знания формул реагентов и продуктов реакции, необходимо верно подобрать коэффициенты.
Это можно сделать, используя несложные правила,
1. Перед формулой простого вещества можно записывать дробный коэффициент, который показывает количество вещества реагирующих и образующихся веществ.
Так, для рассмотренного выше примера:
Н 2 + O 2 → Н 2 O
число атомов кислорода в правой и левой частях уравнения можно сделать равными с помощью коэффициента 1/2, поставив его перед формулой кислорода:
H 2 + 1/2O 2 = H 2 O
Но так как коэффициент показывает не только количество вещества, но и число молекул (атомов), а половину молекулы взять невозможно, лучше переписать приведённое уравнение, удвоив все коэффициенты в нём:
2Н 2 + O 2 = 2Н 2 O.
Приведём ещё пример составления уравнения реакции горения этана С 2 Н 6 , содержащегося в природном газе. Известно, что в результате этого процесса образуются углекислый газ и вода. Схема этой реакции:
С 2 Н 6 + O 2 → СO 2 + Н 2 O.
Уравняем число атомов углерода и водорода:
С 2 Н 6 + O 2 → 2СO 2 + ЗН 2 O.
Теперь в правой части уравнения реакции 7 атомов кислорода, а в левой - только 2. Уравняем число атомов кислорода, записав перед формулой 02 коэффициент 3,5 (7:2 = 3,5):
С 2 Н 6 + 3,5O 2 = 2СO 2 + ЗН 2 O.
И наконец, перепишем полученное уравнение реакции, удвоив коэффициенты перед формулами всех участников реакции:
2С 2 Н 6 + 7O 2 = 4СO 2 + 6Н 2 O.
2. Если в схеме реакции есть формула соли, то вначале уравнивают число ионов, образующих соль.
Например, взаимодействие серной кислоты и гидроксида алюминия описывают схемой:
H 2 SO 4 + Аl(OН) 3 → Al 2 (SO 4) 3 + Н 2 O.
Образующаяся в результате реакции соль - сульфат алюминия Al 2 (SO 4) 3 - состоит из ионов алюминия Аl3+ и сульфат-ионов . Уравняем их число, записав перед формулами H 2 SO 4 и Аl(OН) 3 соответственно коэффициенты 3 и 2:
3H 2 SO 4 + 2Аl(OН) 3 → Al 2 (SO 4) 3 + Н 2 O.
Чтобы уравнять число атомов водорода и кислорода, воспользуемся третьим правилом.
3. Если участвующие в реакции вещества содержат водород и кислород, то атомы водорода уравнивают в предпоследнюю очередь, а атомы кислорода - в последнюю.
Следовательно, уравняем число атомов водорода. В левой части схемы реакции 12 атомов водорода, а в правой - только 2, поэтому перед формулой воды запишем коэффициент 6:
3H 2 SO 4 + 2Аl(OН) 3 → Al 2 (SO 4) 3 + 6Н 2 O.
Индикатором верности расстановки коэффициентов является равенство числа атомов кислорода в левой и правой частях уравнения реакции - по 24 атома кислорода. Поэтому заменим стрелку на знак равенства:
3H 2 SO 4 + 2Аl(OН) 3 = Al 2 (SO 4) 3 + 6Н 2 O.
4. Если в схеме реакции имеется несколько формул солей, то необходимо начинать уравнивание с ионов, входящих в состав соли, содержащей большее их число.
Например, взаимодействие растворов фосфата натрия и нитрата кальция описывают схемой:
Na 3 PO 4 + Ca(NO 3) 2 → Ca 3 (PO 4) 2 + NaNO 3 .
Наибольшее число ионов содержит один из продуктов реакции - фосфат кальция Са 3 (РO 4) 2 , поэтому уравнивают ионы, которыми образована эта соль, - Са 2+ и :
2Na 3 PO 4 + 3Ca(NO 3) 2 → Ca 3 (PO 4) 2 + NaNO 3 .
и, наконец, ионы Na + и N0 - 3:
2Na 3 PO 4 + 3Ca(NO 3) 2 → Ca 3 (PO 4) 2 + 6NaNO 3 .
Ключевые слова и словосочетания
- Химические уравнения.
- Правила подбора коэффициентов в уравнениях реакций.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока - сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Вопросы и задания

Тест по химии Химические уравнения 8 класс с ответами. Тест содержит 2 части. В части 1 — 15 заданий базового уровня. В части 2 — 3 задания повышенного уровня.
Часть 1
1. Верны ли следующие суждения?
А. Масса реагентов равна массе продуктов реакции.
Б. Химическое уравнение — условная запись химической реакции с помощью химических формул и математических знаков.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
2. В ходе химической реакции число атомов некоторого элемента
1) только увеличивается
2) только уменьшается
3) не изменяется
3. В ходе химической реакции число молекул реагентов
1) только увеличивается
2) только уменьшается
3) не изменяется
4) может как увеличиваться, так и уменьшаться
4. В ходе химической реакции число молекул продуктов реакции
1) только увеличивается
2) только уменьшается
3) не изменяется
4) может как увеличиваться, так и уменьшаться
5.
СН 4 + O 2 → СO 2 + Н 2 O.
1) 5
2) 6
3) 7
4) 8
6.
Составьте уравнение реакции по схеме:
FeS + O 2 → Fe 2 O 3 + SO 2 .
1) 13
2) 15
3) 17
4) 19
7.
Составьте уравнение реакции по схеме:
Nа 2 O + Н 2 O → NaOH.
1) 4
2) 5
3) 6
4) 7
8.
Составьте уравнение реакции по схеме:
Н 2 O + N 2 O 5 → HNO 3 .
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 7
2) 6
3) 5
4) 4
9.
Составьте уравнение реакции по схеме:
NаОН + N 2 O 3 → NaNO 2 + Н 2 O.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 7
2) 6
3) 5
4) 4
10.
Составьте уравнение реакции по схеме: Аl 2 O 3 + HCI → AlCl 3 + Н 2 O.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 10
2) 11
3) 12
4) 14
11.
Составьте уравнение реакции по схеме:
Fe(OH) 3 + H 2 SO 4 → Fe 2 (SO 4) 3 + Н 2 O. Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 12
2) 13
3) 14
4) 15
12. Составьте уравнение реакции по схеме:
гидроксид меди (II) + соляная кислота → хлорид меди (II) + вода.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 7
2) 6
3) 5
4) 4
13. Составьте уравнение реакции по схеме:
гидроксид алюминия → оксид алюминия + вода.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 4
2) 5
3) 6
4) 7
14. Составьте уравнение реакции по схеме:
оксид железа (III) + водород → железо + вода.
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 6
2) 7
3) 8
4) 9
15. Составьте уравнение реакции по схеме:
карбонат кальция + соляная кислота → хлорид кальция + вода + оксид углерода (IV).
Ответ дайте в виде суммы коэффициентов в уравнении реакции.
1) 6
2) 7
3) 8
4) 9
Часть 2
1. Установите соответствие между исходными веществами и продуктами соответствующих химических реакций. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту.
Исходные вещества
А) Н 2 + O 2 →
Б) С 2 Н 6 + O 2 →
В) Al(OH) 3 + H 2 SO 4 →
Г) Ca(NO 3) 2 + Na 3 PO 4 →
Продукты реакции
1) СО 2 + Н 2 О
2) Н 2 О
3) Са 3 (РО 4) 2 + NaNO 3
4) Al 2 (SO 4) 3 + Н 2 О
2. Установите соответствие между схемой реакции и суммой коэффициентов в уравнении реакции. Ответ дайте в виде последовательности цифр, соответствующих буквам по алфавиту.
Уравнения реакций
А) Fe 3 O 4 + Аl → Аl 2 O 3 + Fe
Б) Р 2 O 5 + Н 2 О → Н 3 РO 4
В) Al + O 2 → Аl 2 O 3
Г) Fe(OH) 3 → Fe 2 O 3 + Н 2 О
Сумма коэффициентов
1) 6
2) 9
3) 12
4) 18
5) 24
3. Закон сохранения массы вещества является частью более общего закона сохранения материи. Виды материи (энергия и вещество) взаимосвязаны по формуле Эйнштейна: ΔЕ = Δm ⋅ с 2 (где скорость света с = 3 ⋅ 10 8 м/с). Если в ходе реакции, например, выделилось ΔЕ = 90 кДж = 9 ⋅ 10 4 Дж энергии, то масса системы уменьшилась на величину: Δm = ΔЕ/с 2 = 9 ⋅ 10 4 /(3 ⋅ 10 8) 2 = 10 -12 кг = 10 -9 г. Эта величина меньше, чем точность аналитических весов (10 -6 г). Поэтому изменениями массы в ходе химических реакций можно пренебречь. Вычислите величину выделившейся энергии ΔЕ в кДж, если масса системы в ходе реакции уменьшилась на 2,5 ⋅ 10 -9 г. В ответе запишите величину ΔЕ без указания единиц измерения.
Ответы на тест по химии Химические уравнения 8 класс
Часть 1
1-3
2-3
3-2
4-1
5-2
6-3
7-1
8-4
9-2
10-3
11-1
12-2
13-3
14-4
15-1
Часть 2
1-2143
2-5121
3-225
Назад
Вперёд
Внимание! Предварительный просмотр слайдов используется исключительно в ознакомительных целях и может не давать представления о всех возможностях презентации. Если вас заинтересовала данная работа, пожалуйста, загрузите полную версию.
Цель урока: помочь обучающимся сформировать знания о химическом уравнении как об условной записи химической реакции с помощью химических формул.
Задачи:
Образовательные:
- систематизировать ранее изученный материал;
- обучать умению составлять уравнения химических реакций.
Воспитательные:
- воспитывать коммуникативные навыки (работа в паре, умение слушать и слышать).
Развивающие:
- развивать учебно-организационные умения, направленные на выполнение поставленной задачи;
- развивать аналитические навыки мышления.
Тип урока: комбинированный.
Оборудование: компьютер, мультимедийный проектор, экран, оценочные листы, карта рефлексии, “набор химических знаков”, тетрадь с печатной основой, реактивы: гидроксид натрия, хлорид железа(III), спиртовка, держатель, спички, лист ватмана, разноцветные химические знаки.
Презентация урока (приложение 3)
Структура урока.
І. Организационный момент.
ІІ. Актуализация знаний и умений.
ІІІ. Мотивация и целеполагание.
ІV. Изучение нового материала:
4.1 реакция горения алюминия в кислороде;
4.2 реакция разложения гидроксида железа (III);
4.3 алгоритм расстановки коэффициентов;
4.4 минута релаксации;
4.5 расставь коэффициенты;
V. Закрепление полученных знаний.
VІ. Подведение итогов урока и выставление оценок.
VІІ. Домашнее задание.
VІІІ. Заключительное слово учителя.
Ход урока
Химическая натура сложной частицы
определяется натурой элементарных
составных частей,
количеством их и
химическим строением.
Д.И.Менделеев
Учитель.
Здравствуйте, ребята. Садитесь.
Обратите внимание: у вас на столе лежит тетрадь с печатной основой
(Приложение 2),
в которой вы сегодня будете
работать, и оценочный лист, в нем вы будете фиксировать свои достижения,
подпишите его.
Актуализация знаний и умений.
Учитель.
Мы с вами познакомились с физическими и химическими
явлениями, химическими реакциями и признаками их протекания. Изучили закон
сохранения массы веществ.
Давайте проверим ваши знания. Я предлагаю вам открыть тетради с печатной основой
и выполнить задание 1. На выполнение задания вам дается 5 минут.
Тест по теме “Физические и химические явления. Закон сохранения массы веществ”.
1.Чем химические реакции отличаются от физических явлений?
- Изменение формы, агрегатного состояния вещества.
- Образование новых веществ.
- Изменение местоположения.
2. Каковы признаки химической реакции?
- Образование осадка, изменение цвета, выделение газа.
3. В соответствии с каким законом составляются уравнения химических реакций?
- Закон постоянства состава вещества.
- Закон сохранения массы вещества.
- Периодический закон.
- Закон динамики.
- Закон всемирного тяготения.
4. Закон сохранения массы вещества открыл:
- Д.И. Менделеев.
- Ч. Дарвин.
- М.В. Ломоносов.
- И. Ньютон.
- А.И. Бутлеров.
5. Химическим уравнением называют:
- Условную запись химической реакции.
Учитель. Вы выполнили работу. Я предлагаю вам осуществить ее проверку. Поменяйтесь тетрадями и осуществите взаимопроверку. Внимание на экран. За каждый правильный ответ – 1 балл. Общее количество баллов занесите в оценочные листы.
Мотивация и целеполагание.
Учитель. Используя эти знания, мы сегодня будем составлять уравнения химических реакций, раскрывая проблему “Является ли закон сохранения массы веществ основой для составления уравнений химических реакций”
Изучение нового материала.
Учитель. Мы привыкли считать, что уравнение-это математический пример, где есть неизвестное, и это неизвестное нужно вычислить. А вот в химических уравнениях обычно ничего неизвестного не бывает: в них просто записывается все формулами: какие вещества вступают в реакцию и какие получаются в ходе этой реакции. Посмотрим опыт.
(Реакция соединения серы и железа.) Приложение 3
Учитель. С точки зрения массы веществ, уравнение реакции соединения железа и серы понимается следующим образом
Железо + сера → сульфид железа (II) (задание 2 тпо)
Но в химии слова отражаются химическими знаками. Запишите это уравнение химическими символами.
Fe + S → FeS
(Один ученик пишет на доске, остальные в ТПО.)
Учитель.
Теперь прочитайте.
Обучающиеся.
Молекула железа взаимодействует с молекулой серы, получается
одна молекула сульфида железа (II).
Учитель.
В данной реакции мы видим, что количество исходных веществ равно
количеству веществ в продукте реакции.
Всегда надо помнить, что при составлении уравнений реакций ни один атом не
должен потеряться или неожиданно появиться. Поэтому иногда, записав все формулы
в уравнении реакции, приходиться уравнивать число атомов в каждой части
уравнения – расставлять коэффициенты. Посмотрим еще один опыт
(Горение алюминия в кислороде.) Приложение 4
Учитель. Запишем уравнение химической реакции (задание 3 в ТПО)
Al + O 2 → Al +3 O -2
Чтобы записать правильно формулу оксида, вспомним что
Обучающиеся. Кислород в оксидах имеет степень окисления -2, алюминий – химический элемент с постоянной степенью окисления +3. НОК = 6
Al + O 2 → Al 2 O 3
Учитель.
Мы видим, что в реакцию вступает 1 атом алюминия, образуется
два атома алюминия. Вступает два атома кислорода, образуется три атома
кислорода.
Просто и красиво, но неуважительно по отношению к закону сохранения массы
веществ – она разная до и после реакции.
Поэтому нам необходимо расставить коэффициенты в данном уравнении химической
реакции. Для этого найдем НОК для кислорода.
Обучающиеся. НОК = 6
Учитель. Перед формулами кислорода и оксида алюминия ставим коэффициенты, чтобы число атомов кислорода слева и справа было равно 6.
Al + 3 O 2 → 2 Al 2 O 3
Учитель. Теперь получаем, что в результате реакции образуется четыре атома алюминия. Следовательно, перед атомом алюминия в левой части ставим коэффициент 4
Al + 3O 2 → 2Al 2 O 3Еще раз пересчитаем все атомы до реакции и после нее. Ставим равно.
4Al + 3O 2 _ = 2 Al 2 O 3
Учитель. Рассмотрим еще один пример
(Учитель демонстрирует опыт по разложению гидроксида железа (III).)
Fe(OH) 3 → Fe 2 O 3 + H 2 O
Учитель. Расставим коэффициенты. В реакцию вступает 1 атом железа, образуется два атома железа. Следовательно, перед формулой гидроксида железа (3) ставим коэффициент 2.
Fe(OH) 3 → Fe 2 O 3 + H 2 OУчитель. Получаем, что в реакцию вступает 6 атомов водорода (2х3), образуется 2 атома водорода.
Обучающиеся. НОК =6. 6/2 = 3. Следовательно, у формулы воды ставим коэффициент 3
2Fe(OH) 3 → Fe 2 O 3 + 3 H 2 O
Учитель. Считаем кислород.
Обучающиеся. Слева – 2х3 =6; справа – 3+3 = 6
Обучающиеся. Количество атомов кислорода,вступивших в реакцию, равно количеству атомов кислорода, образовавшихся в ходе реакции. Можно ставить равно.
2Fe(OH) 3 = Fe 2 O 3 +3 H 2 O
Учитель. Теперь давайте обобщим все сказанное ранее и познакомимся с алгоритмом расстановки коэффициентов в уравнениях химических реакций.
- Подсчитать количество атомов каждого элемента в правой и левой части уравнения химической реакции.
- Определить, у какого элемента количество атомов меняется, найти НОК.
- Разделить НОК на индексы – получить коэффициенты. Поставить их перед формулами.
- Пересчитать количество атомов, при необходимости действие повторить.
- Последним проверить количество атомов кислорода.
Учитель.
Вы хорошо потрудились и, наверное, устали. Я предлагаю вам
расслабиться, закрыть глаза и вспомнить какие-либо приятные моменты жизни. У
каждого из вас они разные. Теперь откройте глаза и сделайте круговые движения
ими сначала по часовой стрелке, затем – против. Теперь интенсивно подвигайте
глазами по горизонтали: направо – налево, и вертикали: вверх – вниз.
А сейчас активизируем мыслительную деятельность и помассируем мочки ушей.
Учитель.
Продолжаем работу.
В тетрадях с печатной основой выполним задание 5. Работать вы будете в парах.
Вам необходимо расставить коэффициенты в уравнених химических реакций. На
выполнение задания дается 10 минут.
- P + Cl 2 →PCl 5
- Na + S → Na 2 S
- HCl + Mg →MgCl 2 + H 2
- N 2 + H 2 →NH 3
- H 2 O → H 2 + O 2
Учитель.
Проверим выполнение задания (учитель опрашивает и выводит
на слайд правильные ответы)
. За каждый правильно поставленный коэффициент –
1 балл.
С заданием вы справились. Молодцы!
Учитель.
Теперь давайте вернемся к нашей проблемы.
Ребята, как вы считаете, является ли закон сохранения массы веществ основой для
составления уравнений химических реакций.
Обучающиеся. Да, в ходе урока мы доказали, что закон сохранения массы веществ – основа для составления уравнений химических реакций.
Закрепление знаний.
Учитель. Все основные вопросы мы изучили. Теперь выполним небольшой тест, который позволит увидеть, как вы освоили тему. Вы должны на него отвечать только “да” или “нет”. На работу дается 3 минуты.
Утверждения.
- В реакции Ca + Cl 2 → CaCl 2 коэффициенты не нужны. (Да)
- В реакции Zn + HCl → ZnCl 2 + H 2 коэффициент у цинка 2. (Нет)
- В реакции Ca + O 2 → CaO коэффициент у оксида кальция 2. (Да)
- В реакции CH 4 → C + H 2 коэффициенты не нужны. (Нет)
- В реакции CuO + H 2 → Cu + H 2 O коэффициент у меди 2. (Нет)
- В реакции C + O 2 → CO коэффициент 2 надо поставить и у оксида углерода (II) , и у углерода. (Да)
- В реакции CuCl 2 + Fe → Cu + FeCl 2 коэффициенты не нужны. (Да)
Учитель. Проверим выполнение работы. За каждый правильный ответ – 1 балл.
Итог урока.
Учитель. Вы справились хорошо с заданием. Сейчас подсчитайте общее количество набранных баллов за урок и поставьте себе оценку согласно рейтингу, который вы видите на экране. Сдайте мне оценочные листы для выставления вашей оценки в журнал.
Домашнее задание.
Учитель. Наш урок подошел к концу, в ходе которого мы смогли доказать, что закон сохранения массы веществ является основой для составления уравнений реакций, и научились составлять уравнения химических реакций. И, как финальная точка, запишите домашнее задание
§ 27, упр. 1 – для тех, кто получил оценку “3”
упр. 2– для тех, кто получил оценку “4”
упр. 3 – для тех, кто получил оценку
“5”
Заключительное слово учителя.
Учитель. Я благодарю вас за урок. Но прежде чем вы покинете кабинет, обратите внимание на таблицу (учитель показывает на лист ватмана с изображением таблицы и разноцветными химическими знаками). Вы видите химические знаки разного цвета. Каждый цвет символизирует ваше настроение.. Я предлагаю вам составить свою таблицу химических элементов (она будет отличаться от ПСХЭ Д.И.Менделеева) – таблицу настроения урока. Для этого вы должны подойти к нотному листу, взять один химический элемент, согласно той характеристике, которую вы видите на экране, и прикрепить в ячейку таблицы. Я сделаю это первой, показав вам свою комфортность от работы с вами.
F Мне было на уроке комфортно, я получил ответ на все интересующие меня
вопросы.
F Мне на уроке было скучно, я ничего не узнал нового .
В уроке 13 «» из курса «Химия для чайников » рассмотрим для чего нужны химические уравнения; научимся уравнивать химические реакции, путем правильной расстановки коэффициентов. Данный урок потребует от вас знания химических основ из прошлых уроков. Обязательно прочитайте об элементном анализе, где подробно рассмотрены эмпирические формулы и анализ химических веществ.
В результате реакции горения метана CH 4 в кислороде O 2 образуются диоксид углерода CO 2 и вода H 2 O. Эта реакция может быть описана химическим уравнением :
- CH 4 + O 2 → CO 2 + H 2 O (1)
Попробуем извлечь из химического уравнения больше сведений, чем просто указание продуктов и реагентов реакции. Химичекое уравнение (1) является НЕполным и потому не дает никаких сведений о том, сколько молекул O 2 расходуется в расчете на 1 молекулу CH 4 и сколько молекул CO 2 и H2 O получается в результате. Но если записать перед соответствующими молекулярными формулами численные коэффициенты, которые укажут сколько молекул каждого сорта принимает участие в реакции, то мы получим полное химическое уравнение реакции.
Для того, чтобы завершить составление химического уравнения (1), нужно помнить одно простое правило: в левой и правой частях уравнения должно присутствовать одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожение имевшихся. Данное правило основывается на законе сохранения массы, который мы рассмотрели в начале главы.
Нужно для того, чтобы из простого химического уравнения получить полное. Итак, перейдем к непосредственному уравниванию реакции (1): еще раз взгляните на химическое уравнение, в точности на атомы и молекулы в правой и левой части. Нетрудно заметить, что в реакции участвуют атомы трех сортов: углерод C, водород H и кислород O. Давайте подсчитаем и сравним количество атомов каждого сорта в правой и левой части химического уравнения.
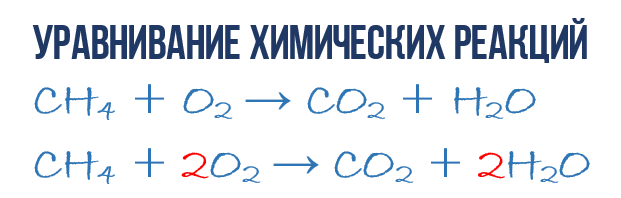
Начнем с углерода. В левой части один атом С входит в состав молекулы CH 4 , а в правой части один атом С входит в состав CO 2 . Таким образом в левой и в правой части количество атомов углерода совпадает, поэтому его мы оставляем в покое. Но для наглядности поставим коэффициент 1 перед молекулами с углеродом, хоть это и не обязательно:
- 1CH 4 + O 2 → 1CO 2 + H 2 O (2)
Затем переходим к подсчету атомов водорода H. В левой части присутствуют 4 атома H (в количественном смысле H 4 = 4H) в составе молекулы CH 4 , а в правой – всего 2 атома H в составе молекулы H 2 O, что в два раза меньше чем в левой части химического уравнения (2). Будем уравнивать! Для этого поставим коэффициент 2 перед молекулой H 2 O. Вот теперь у нас и в реагентах и в продуктах будет по 4 молекулы водорода H:
- 1CH 4 + O 2 → 1CO 2 + 2H 2 O (3)
Обратите свое внимание, что коэффициент 2, который мы записали перед молекулой воды H 2 O для уравнивания водорода H, увеличивает в 2 раза все атомы, входящие в ее состав, т.е 2H 2 O означает 4H и 2O. Ладно, с этим вроде бы разобрались, осталось подсчитать и сравнить количество атомов кислорода O в химическом уравнении (3). Сразу бросается в глаза, что в левой части атомов O ровно в 2 раза меньше чем в правой. Теперь-то вы уже и сами умеете уравнивать химические уравнения, поэтому сразу запишу финальный результат:
- 1CH 4 + 2O 2 → 1CO 2 + 2H 2 O или СH 4 + 2O 2 → CO 2 + 2H 2 O (4)
Как видите, уравнивание химических реакций не такая уж и мудреная штука, и важна здесь не химия, а математика. Уравнение (4) называется полным уравнением химической реакции, потому что в нем соблюдается закон сохранения массы, т.е. число атомов каждого сорта, вступающих в реакцию, точно совпадает с числом атомов данного сорта по завершении реакции. В каждой части этого полного химического уравнения содержится по 1 атому углерода, по 4 атома водорода и по 4 атома кислорода. Однако стоит понимать пару важных моментов: химическая реакция — это сложная последовательность отдельных промежуточных стадий, и потому нельзя к примеру истолковывать уравнение (4) в том смысле, что 1 молекула метана должна одновременно столкнуться с 2 молекулами кислорода. Процессы происходящие при образовании продуктов реакции гораздо сложнее. Второй момент: полное уравнение реакции ничего не говорит нам о ее молекулярном механизме, т.е о последовательности событий, которые происходят на молекулярном уровне при ее протекании.
Коэффициенты в уравнениях химических реакций
Еще один наглядный пример того, как правильно расставить коэффициенты в уравнениях химических реакций: Тринитротолуол (ТНТ) C 7 H 5 N 3 O 6 энергично соединяется с кислородом, образуя H 2 O, CO 2 и N 2 . Запишем уравнение реакции, которое будем уравнивать:
- C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (5)
Проще составлять полное уравнение, исходя из двух молекул ТНТ, так как в левой части содержится нечетное число атомов водорода и азота, а в правой — четное:
- 2C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (6)
Тогда ясно, что 14 атомов углерода, 10 атомов водорода и 6 атомов азота должны превратиться в 14 молекул диоксида углерода, 5 молекул воды и 3 молекулы азота:
- 2C 7 H 5 N 3 O 6 + O 2 → 14CO 2 + 5H 2 O + 3N 2 (7)
Теперь в обеих частях содержится одинаковое число всех атомов, кроме кислорода. Из 33 атомов кислорода, имеющихся в правой части уравнения, 12 поставляются двумя исходными молекулами ТНТ, а остальные 21 должны быть поставлены 10,5 молекулами O 2 . Таким образом полное химическое уравнение будет иметь вид:
- 2C 7 H 5 N 3 O 6 + 10,5O 2 → 14CO 2 + 5H 2 O + 3N 2 (8)
Можно умножить обе части на 2 и избавиться от нецелочисленного коэффициента 10,5:
- 4C 7 H 5 N 3 O 6 + 21O 2 → 28CO 2 + 10H 2 O + 6N 2 (9)
Но этого можно и не делать, поскольку все коэффициенты уравнения не обязательно должны быть целочисленными. Правильнее даже составить уравнение, исходя из одной молекулы ТНТ:
- C 7 H 5 N 3 O 6 + 5,25O 2 → 7CO 2 + 2,5H 2 O + 1,5N 2 (10)
Полное химическое уравнение (9) несет в себе много информации. Прежде всего оно указывает исходные вещества — реагенты , а также продукты реакции. Кроме того, оно показывает, что в ходе реакции индивидуально сохраняются все атомы каждого сорта. Если умножить обе части уравнения (9) на число Авогадро N A =6,022·10 23 , мы сможем утверждать, что 4 моля ТНТ реагируют с 21 молями O 2 с образованием 28 молей CO 2 , 10 молей H 2 O и 6 молей N 2 .
Есть еще одна фишка. При помощи таблицы Менделеева определяем молекулярные массы всех этих веществ:
- C 7 H 5 N 3 O 6 = 227,13 г/моль
- O2 = 31,999 г/моль
- CO2 = 44,010 г/моль
- H2 O = 18,015 г/моль
- N2 = 28,013 г/моль
Теперь уравнение 9 укажет еще, что 4·227,13 г = 908,52 г ТНТ требуют для осуществления полной реакции 21·31,999 г = 671,98 г кислорода и в результате образуется 28·44,010 г = 1232,3 г CO 2 , 10·18,015 г = 180,15 г H 2 O и 6·28,013 г = 168,08 г N 2 . Проверим, выполняется ли в этой реакции закон сохранения массы:
| Реагенты | Продукты | |
| 908,52 г ТНТ | 1232,3 г CO2 | |
| 671,98 г CO2 | 180,15 г H2 O | |
| 168,08 г N2 | ||
| Итого | 1580,5 г | 1580,5 г |
Но необязательно в химической реакции должны участвовать индивидуальные молекулы. Например, реакция известняка CaCO3 и соляной кислоты HCl, с образованием водного раствора хлорида кальция CaCl2 и диоксида углерода CO2 :
- CaCO 3 + 2HCl → CaCl 2 + CO 2 + H 2 O (11)
Химическое уравнение (11) описывает реакцию карбоната кальция CaCO 3 (известняка) и хлористоводородной кислоты HCl с образованием водного раствора хлорида кальция CaCl 2 и диоксида углерода CO 2 . Это уравнение полное, так как число атомов каждого сорта в его левой и правой частях одинаково.
Смысл этого уравнения на макроскопическом (молярном) уровне таков: 1 моль или 100,09 г CaCO 3 требует для осуществления полной реакции 2 моля или 72,92 г HCl, в результате чего получается по 1 молю CaCl 2 (110,99 г/моль), CO 2 (44,01 г/моль) и H 2 O (18,02 г/моль). По этим численным данным нетрудно убедиться, что в данной реакции выполняется закон сохранения массы.
Интерпретация уравнения (11) на микроскопическом (молекулярном) уровне не столь очевидна, поскольку карбонат кальция представляет собой соль, а не молекулярное соединение, а потому нельзя понимать химическое уравнение (11) в том смысле, что 1 молекула карбоната кальция CaCO 3 реагирует с 2 молекулами HCl. Тем более молекула HCl в растворе вообще диссоциирует (распадается) на ионы H + и Cl — . Таким образом более правильным описанием того, что происходит в этой реакции на молекулярном уровне, дает уравнение:
- CaCO 3 (тв.) + 2H + (водн.) → Ca 2+ (водн.) + CO 2 (г.) + H 2 O(ж.) (12)
Здесь в скобках сокращенно указано физическое состояние каждого сорта частиц (тв. — твердое, водн. — гидратированный ион в водном растворе, г. — газ, ж. — жидкость).
Уравнение (12) показывает, что твердый CaCO 3 реагирует с двумя гидратированными ионами H + , образуя при этом положительный ион Ca 2+ , CO 2 и H 2 O. Уравнение (12) как и другие полные химические уравнения не дает представления о молекулярном механизме реакции и менее удобно для подсчета количества веществ, однако, оно дает лучшее описание происходящего на микроскопическом уровне.
Закрепите полученные знания о составлении химических уравнений, самостоятельно разобрав пример с решением:
Надеюсь из урока 13 «Составление химических уравнений » вы узнали для себя что-то новое. Если у вас возникли вопросы, пишите их в комментарии.





